2026 ELCC丨从后线突破到一线布局:刘海峰教授解读国产HER3 ADC YL202/BNT326在NSCLC中的重磅数据与国际化征程
来源: 时间:2026-04-09 浏览: 次

2026年欧洲肺癌大会(ELCC)于3月25日至28日在丹麦哥本哈根盛大召开。作为胸部肿瘤学领域的国际顶级盛会,ELCC汇聚了全球前沿的科研成果与临床智慧。在本届大会上,来自中国的多项研究再次成为焦点,其中,来自吉林省肿瘤医院刘海峰教授主持开展的一项关于HER3靶向抗体药物偶联物(ADC)YL202/BNT326的II期临床试验(YL202-CN-201-01,NCT06107686)以口头报告形式首次公布了其在非小细胞肺癌(NSCLC)患者中的疗效与安全性数据。会议现场,《肿瘤瞭望》特邀刘海峰教授接受专访,深入解读了该研究对临床实践的启示、安全性特征以及国产创新药的国际化征程。

刘海峰教授
研究介绍
研究背景
在非小细胞肺癌(NSCLC)的治疗中,HER3(人表皮生长因子受体3)广泛表达,且与肿瘤进展及治疗耐药密切相关,尤其在EGFR突变(EGFRm)患者中,HER3已成为重要的治疗靶点。抗体药物偶联物(ADC)的发展为克服耐药提供了新思路。YL202/BNT326是一种新型HER3靶向ADC,本研究首次在II期临床试验中系统评估其在多线治疗后的NSCLC患者中的疗效与安全性,涵盖EGFR突变、鳞状及非鳞状无驱动基因突变(AGA-neg)等多个亚型,填补了HER3 ADC在部分人群中的数据空白。

研究方法
本研究(YL202-CN-201-01,NCT06107686)为一项多中心、开放标签、II期临床试验,全部患者均来自中国。研究共纳入152例晚期NSCLC患者,分为三个主要队列:
队列A2(EGFRm NSCLC):102例患者,既往接受过TKI和铂类化疗(PBC),分别接受2.0 mg/kg、2.5 mg/kg或3.0 mg/kg的YL202/BNT326静脉给药,每3周一次。
队列E1(鳞状NSCLC):23例患者,既往接受过1–2线治疗(必须包含PD-(L)1抑制剂±化疗),仅评估2.0 mg/kg剂量。
队列E2(非鳞状、AGA-neg NSCLC):27例患者,既往接受过1–2线治疗(必须包含PD-(L)1抑制剂±化疗),接受2.0 mg/kg、2.5 mg/kg或3.0 mg/kg剂量。
主要终点为研究者评估的客观缓解率(ORR)及推荐剂量,次要终点包括无进展生存期(PFS)、疾病控制率(DCR)、缓解持续时间(DoR)和安全性。数据截止日期为2026年1月27日,中位随访时间为10.6个月,29例患者仍在治疗中。
研究结果
患者基线特征:共纳入152例患者,各队列患者基线特征显示其均为高度异质且经多线治疗的人群:
EGFRm队列:中位年龄57.5岁,86.3%的患者ECOG PS评分为1分,54.9%存在Exon 19缺失,50.0%存在L858R突变。中位既往治疗线数为3线,90.2%既往接受过三代EGFR-TKI治疗,全部患者接受过铂类化疗,27.5%接受过PD-(L)1抑制剂。
鳞状NSCLC队列:中位年龄66.0岁,中位既往治疗线数为1线,全部患者接受过PD-(L)1抑制剂,91.3%接受过紫杉类治疗。
非鳞状、AGA-neg队列:中位年龄57.0岁,中位既往治疗线数为2线,全部患者接受过PD-(L)1抑制剂,77.8%接受过铂类化疗。

疗效结果:
EGFR突变NSCLC(3线及以上治疗)
共96例患者纳入疗效分析。在2.0 mg/kg、2.5 mg/kg和3.0 mg/kg三个剂量组中:确认的ORR分别为27.3%、26.7%和48.5%,总体ORR为34.4%;疾病控制率(DCR)分别为90.9%、83.3%和93.9%,总体DCR为89.6%;中位DoR分别为6.9个月、8.4个月和6.8个月,总体中位DoR为7.0个月;中位PFS分别为8.1个月、7.1个月和8.2个月,总体中位PFS为7.5个月;6个月PFS率分别为54.3%、58.9%和65.9%,总体为59.6%。

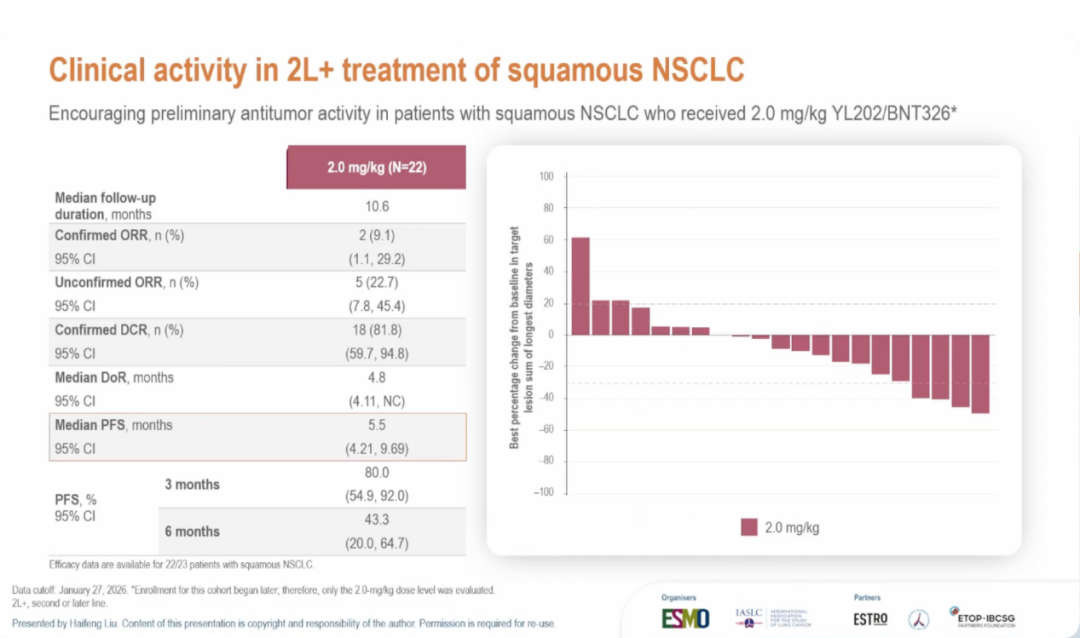
鳞状NSCLC(2线及以上治疗)
22例患者接受2.0 mg/kg治疗,中位随访10.6个月:确认ORR为9.1%,DCR为81.8%;中位DoR为4.8个月,中位PFS为5.5个月;6个月PFS率为43.3%。
非鳞状、AGA-neg NSCLC(2线及以上治疗)
27例患者接受不同剂量治疗:
2.0 mg/kg组(15例)确认ORR为46.7%,DCR为100%;中位PFS为5.6个月。
3.0 mg/kg组(9例)确认ORR为33.3%,DCR为66.7%;中位PFS为8.2个月。
总体确认ORR为37.0%,总体DCR为88.9%,总体中位PFS为5.6个月。

安全性结果:YL202/BNT326总体耐受性良好。治疗相关不良事件(TRAEs)主要为血液学及胃肠道反应,多为1–2级。在2.0 mg/kg和2.5 mg/kg剂量组中,治疗中断率较低(分别为4.2%和2.7%)。药物相关间质性肺病(ILD)发生率为2.6%(4例),其中3例为1–2级,1例为3级。仅1例患者因治疗相关肺炎死亡(2.0 mg/kg组)。


研究结论
本研究首次系统报道了HER3 ADC YL202/BNT326在多种NSCLC亚型中的疗效与安全性数据。研究结果表明:
在EGFR突变NSCLC患者中,YL202/BNT326在3线及以上治疗中显示出稳健的缓解率和持久疾病控制,2.0 mg/kg剂量下中位PFS达8.1个月,该剂量已推进至III期研究。
在非鳞状、无驱动基因突变NSCLC患者中,2.0 mg/kg剂量下确认ORR达46.7%,为HER3 ADC在该人群中的首次数据披露。
在鳞状NSCLC患者中,本研究首次报告了HER3靶向ADC的临床活性,中位PFS为5.5个月,疾病控制率达81.8%,填补了该领域的重要空白。
安全性方面,YL202/BNT326在2.0 mg/kg和2.5 mg/kg剂量下表现良好,不良事件可控,治疗终止率低,支持其后续单药及联合治疗的临床开发。
目前,YL202/BNT326单药在EGFR突变NSCLC患者中的III期研究(NCT07416994)以及联合PD-L1×VEGF-A双特异性抗体pumitinib的研究(NCT07111520)正在进行中,进一步探索其在NSCLC治疗中的应用前景。
研究者说
刘海峰 教授
研究结果解读与临床启示
刘海峰教授首先介绍了YL202/BNT326的研发背景。他指出,YL202是一款基于宜联生物独特ADC技术平台研发的新型HER3靶向ADC,由宜联生物与BioNTech共同推进全球临床开发。本次公布的II期数据是该药物在NSCLC领域的首次系统披露,研究覆盖了EGFR突变、驱动基因阴性非鳞癌及鳞癌等多种亚型,为HER3 ADC在不同人群中的应用提供了重要循证依据。
刘教授强调,在经TKI及含铂化疗治疗后的EGFR突变NSCLC患者中,YL202在选定的III期推荐剂量(2.0 mg/kg)下,中位PFS达到8.1个月,显示出稳健且持久的抗肿瘤活性。基于此,该人群已顺利进入III期确证性研究(NCT07416994)。而在驱动基因阴性的非鳞状NSCLC患者中,YL202同样展现出令人鼓舞的疗效,确认ORR高达46.7%,为这一后线治疗选择极为有限的人群带来了全新的治疗希望。目前,针对该人群的YL202联合PD-L1/VEGF双抗(pumitamig,BNT327)的一线治疗研究已进入全球II期探索阶段,未来有望进一步前移治疗线序。
差异化安全性优势与患者管理价值
谈及安全性,刘海峰教授指出,YL202展现了与同类药物相比明显差异化的安全性优势。在当前ADC药物普遍面临血液学毒性及黏膜炎挑战的背景下,YL202通过II期试验中充分的剂量探索,在2.0 mg/kg剂量下真正实现了“低毒高效”的研发目标。
具体数据显示,在该剂量水平下,≥3级的贫血、中性粒细胞减少及血小板减少发生率均低于5%,任意级别的黏膜炎发生率仅约10%。这一安全性特征对于需要长期疾病管理的晚期肺癌患者而言意义重大,意味着YL202将是一款耐受性极佳的ADC药物,有望在保证疗效的同时,显著提升患者的生活质量及治疗依从性。
国产创新药的国际化布局与未来展望
谈及国产创新药在国际舞台的地位,刘海峰教授表示,本次ELCC大会既是ADC单药研究成果的集中展示,也标志着联合治疗策略的全面兴起。相较于国际同类研究,YL202是基于宜联生物自主研发的ADC技术平台、并与德国BioNTech共同推进全球临床开发的一款HER3靶向ADC,其研发路径充分体现了中国创新药从“跟跑”、“并跑”到“领跑”的跨越。
刘教授介绍,YL202的全球开发策略具备三大特点:其一,在I/II期阶段即开展了充分的剂量探索,确定了最佳的疗效-安全性平衡点;其二,积累了国际多中心、多瘤种、多人种的数百例临床数据,为全球注册奠定了基础;其三,同步推进ADC单药与联合治疗的临床布局,形成了后线与前线并进、单药与联合互补的立体化研发格局。
在具体推进策略上,YL202已在经TKI和含铂化疗后的EGFR突变NSCLC后线治疗中启动III期临床试验;同时,联合PD-L1/VEGF双抗用于驱动基因阴性非鳞癌一线治疗的II期研究正在进行,后续将与FDA及CDE沟通后启动全球III期试验;此外,联合TKI用于一线EGFR突变NSCLC的布局也在积极规划中。
刘海峰教授最后总结道,随着上述临床试验的持续推进,YL202有望凭借其更低的血液学毒性、更低的黏膜炎发生率,为临床医生提供一种高效且耐受性优异的治疗新选择,为非小细胞肺癌患者带来更多临床获益。
刘海峰 教授
主任医师,博士生导师
吉林省肿瘤医院党委书记
吉林省抗癌协会理事长
吉林省癌症中心主任
吉林省肿瘤医院药物临床试验机构主任
吉林省肿瘤医院肿瘤转化医学实验室主任
中国医院协会肿瘤医院分会常委
中国抗癌协会整合肿瘤心脏病学分会常委
吉林省抗癌协会整合肿瘤心脏病专业委员会主任委员
吉林省药学会临床试验专业委员会副主任委员
全国先进工作者、全国优秀党务工作者、《中国卫生》“推进医改,服务百姓健康”十大新闻人物



参考文献:
Haifeng Liu, et al. First disclosure of efficacy and safety data for YL202/BNT326 (HER3 ADC) from a phase II trial in patients (pts) with non-small cell lung cancer (NSCLC). 2026 ELCC. 11MO
(转载来源:《肿瘤瞭望》)

