难治性 NSCLC 后线中位 PFS 超 8 个月! 中国原研 HER3 ADC 闪耀 ELCC
来源: 时间:2026-04-03 浏览: 次
| 转载自:丁香园肿瘤时间
2026 年欧洲肺癌大会(ELCC)于 3 月 25 日至 28 日在丹麦哥本哈根盛大召开,作为全球肺癌领域最具影响力的学术会议之一,本届 ELCC 汇聚了世界各地的顶尖专家与学者,共同探讨肺癌最新临床研究进展,推动肺癌诊疗不断向精准化与个体化方向迈进。
本届 ELCC 现场,吉林省肿瘤医院刘海峰教授现场汇报了 YL202/BNT326 单药治疗非小细胞肺癌(NSCLC)的首次临床疗效数据。这项正在进行的 II 期研究涵盖了表皮生长因子突变(EGFR)突变、鳞状及无可靶向基因组改变(AGA)的非鳞状 NSCLC 患者,显示了 YL202/BNT326 单药在不同 NSCLC 亚组中的抗肿瘤活性及安全性特征,不仅为后线 NSCLC 患者提供了潜在的治疗新选择,更为后续联合免疫治疗的探索奠定了坚实基础。「丁香园肿瘤时间」特邀请刘海峰教授围绕该研究进行了深入探讨,并整理如下,旨在与各位读者一同学习交流。
本研究旨在评估 YL202/BNT326 单药在难治性实体瘤患者中的初步疗效和安全性。其中,NSCLC 是全球癌症相关死亡的主要原因之一,尽管当前靶向治疗和免疫治疗取得了显著进展,但后线治疗选择仍然有限,尤其是对于一线标准治疗失败后的 EGFR 突变及无 AGA 突变患者,临床存在未被满足的需求。
YL202/BNT326 是一款在研的人表皮生长因子受体 -3(HER3)靶向抗体偶联药物(ADC),通过三肽连接子偶联了 8 个新型拓扑异构酶 I 抑制剂载荷(药物 / 抗体比 [DAR] 8)分子,具有高载药量和强效杀伤等特点。刘海峰教授本次汇报报告了 II 期试验中 YL202/BNT326 单药治疗后疾病进展的 NSCLC 患者(EGFR 突变 / 伴或不伴 AGA)的首次临床疗效数据,为后续联合免疫治疗的 III 期临床研究开展提供了关键数据支持。
本研究是一项在中国开展的多中心、开放标签的 II 期临床研究,旨在评估 YL202/BNT326 对晚期实体瘤患者的疗效、安全性和药代动力学特征。其中,NSCLC 队列纳入了 152 例中国 NSCLC 患者,并根据 NSCLC 亚型及既往治疗线数将患者分层,接受 2.0 mg/kg 、2.5 mg/kg 或 3.0 mg/kg YL202/BNT326 单药治疗,每 3 周一次。
研究的主要终点为客观缓解率(ORR)和确定的推荐剂量,次要终点包括无进展生存期(PFS)、疾病控制率(DCR)、缓解持续时间(DoR)及安全性评估。
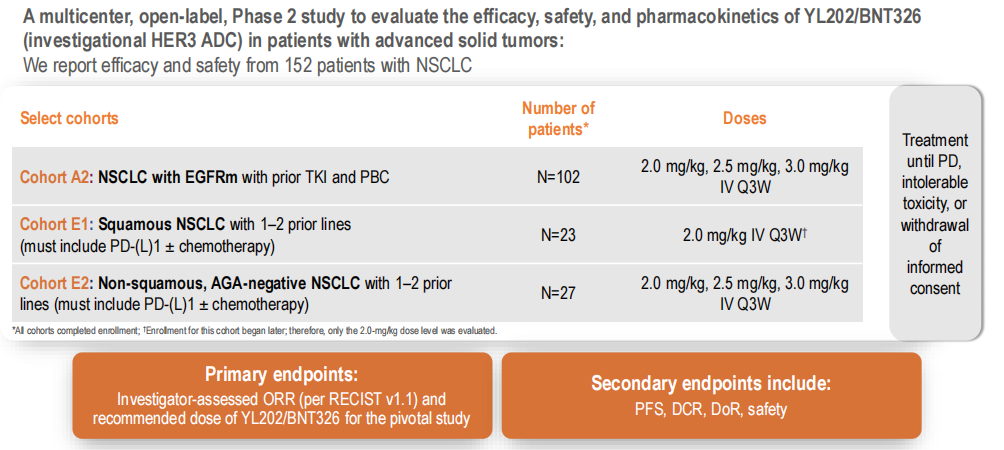
图 1、患者分层及治疗方案
患者基线特征
本研究共纳入 152 例既往接受过 1-2 线标准治疗后出现疾病进展的 NSCLC 患者(EGFR 突变组 102 例,鳞癌组 23 例,非鳞癌组 27 例)。患者基线特征显示,EGFR 突变组患者中位年龄为 57.5 岁,鳞癌组患者为 66.0 岁,非鳞癌组患者为 57.0 岁;各组中 ECOG PS 评分为 1 分的患者占比分别为 86.3%、78.3% 和 88.9%。此外,在 EGFR 突变组中,外显子 19 缺失突变占 54.9%,L858R 突变占 50.0%。脑转移在 EGFR 突变组中最为常见,发生率为 25.5%。
治疗方面,EGFR 突变组患者中位既往治疗线数为 3 线,所有患者(100%)均接受过铂类化疗,其中 90.2% 接受过三代 EGFR 酪氨酸激酶抑制剂(TKI)治疗;鳞癌组和非鳞癌组患者均 100% 接受过程序性死亡受体 / 配体 -1(PD-1/PD-L1)抑制剂治疗。入组后,所有患者均接受了至少一剂 YL202/BNT326 治疗(剂量为 2.0 mg/kg 、2.5 mg/kg 或 3.0 mg/kg,Q3W)。
主要疗效数据:各亚组 NSCLC ORR 均获益显著
截至 2025 年 10 月 27 日,研究中位随访时间为 7.8 个月。在 96 例可评估疗效的 EGFR 突变 NSCLC 患者中,YL202/BNT326 单药三线及以上治疗的 ORR 为 41.7%(95% CI: 31.7%-52.2%),确认客观缓解率(cORR)为 34.4%(95% CI: 25.0%-44.8%),确认 cDCR 达 86%,中位 PFS 为 7.5 个月(95% CI: 5.91 个月 -8.84 个月)。
剂量亚组进一步分析显示,3.0 mg/kg 剂量组的 ORR 达 51.5%(cORR 达 48.5%),数值上优于 2.0 mg/kg 剂量组的 33.3%(cORR 为 27.3%),但在 PFS 方面,2.0 mg/kg 与 3.0 mg/kg 剂量组表现相当,分别为 8.1 个月和 8.2 个月;且两组均显示出持久的缓解,中位 DoR 分别为 6.9 个月和 6.8 个月。
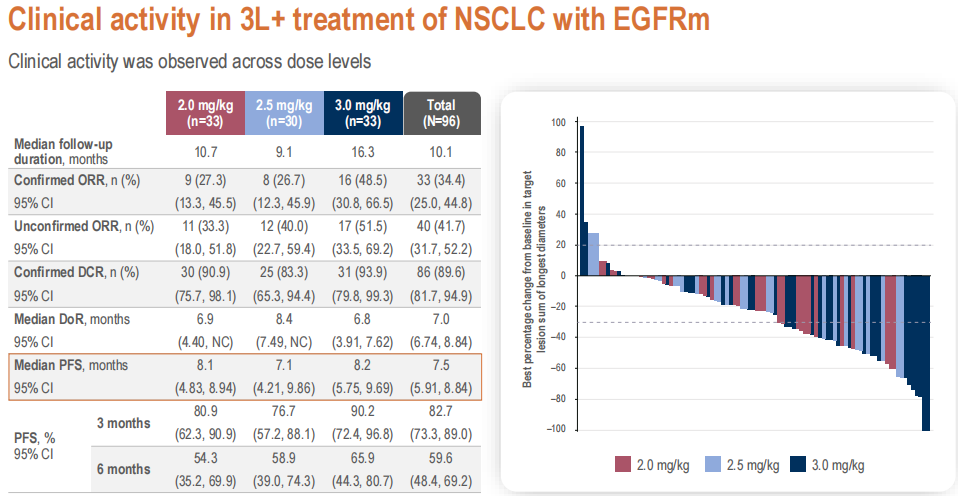
图 2、EGFR 突变 NSCLC 队列疗效数据
此外,在鳞状 NSCLC(n=22)和 AGA 阴性非鳞状 NSCLC 队列(n=27)中,YL202/BNT326 单药二线及以上治疗 ORR 分别为 22.7%(95% CI:7.8%-45.4%)和 48.1%(95% CI: 28.7%-68.1%),cORR 分别为 9.1%(95% CI:1.1%-29.2%)和 37.0%(95% CI:19.4%-57.6%),中位 PFS 分别为 5.5 个月(4.21 个月 -9.69 个月)和 5.6 个月(5.39 个月 -8.34 个月)。
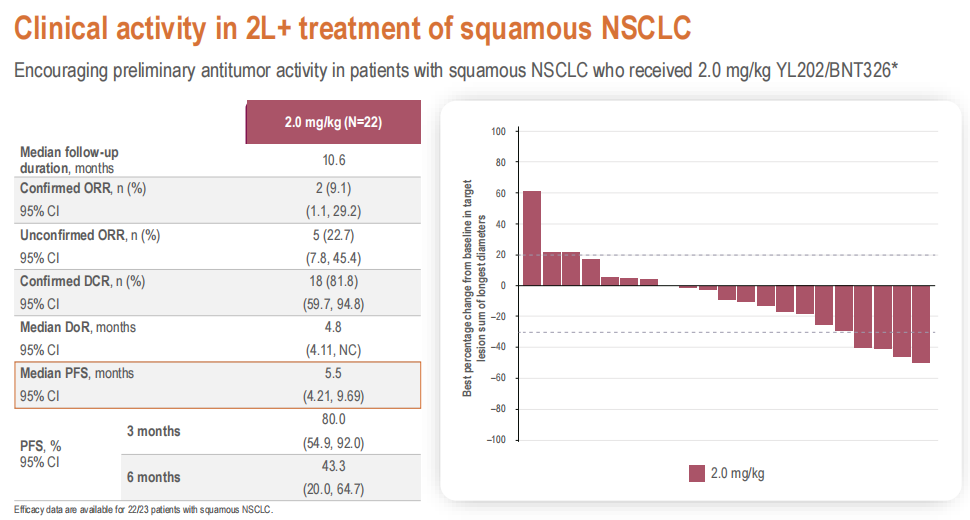
图 3、鳞状 NSCLC 队列疗效数据
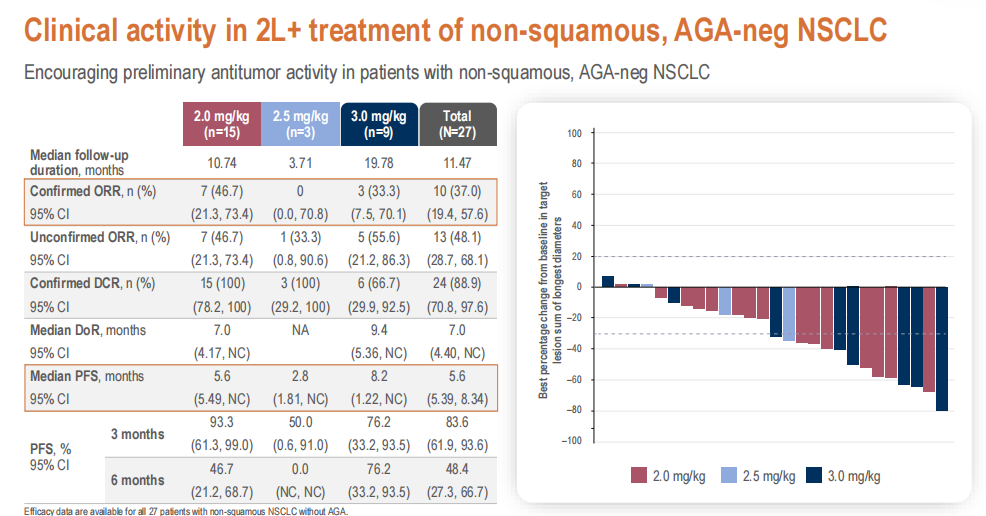
图 4、AGA 阴性、非鳞状 NSCLC 队列疗效数据
安全性分析:2.0 mg/kg 和 2.5 mg/kg 剂量下整体耐受性良好
安全性方面,97.4% 的患者发生了治疗相关不良事件(TRAEs),主要包括贫血(67.8%)、恶心(44.7%)和食欲下降(43.4%)等,但治疗中断率较低,仅 8 例(5.3%)患者因 TRAEs 停药,尤其以 2.0 mg/kg 和 2.5 mg/kg 剂量组耐受性更佳。此外,≥3 级 TRAEs 在 2.0 mg/kg、2.5 mg/kg、3.0 mg/kg 剂量组中发生率分别为 30.6%、48.6%、55.8%,1 例患者死于肺炎(2.0 mg/kg 剂量组)。
在需注意的不良事件方面,≥3 级中性粒细胞减少(8.6%)、白细胞计数减少(7.6%)发生率较低,且仅报告了 1 例间质性肺病(ILD),提示该药物具有相对可控的安全性特征,尤其是低发的 ILD 和中性粒细胞减少症为其临床应用提供了良好基础。
表 1、安全性分析
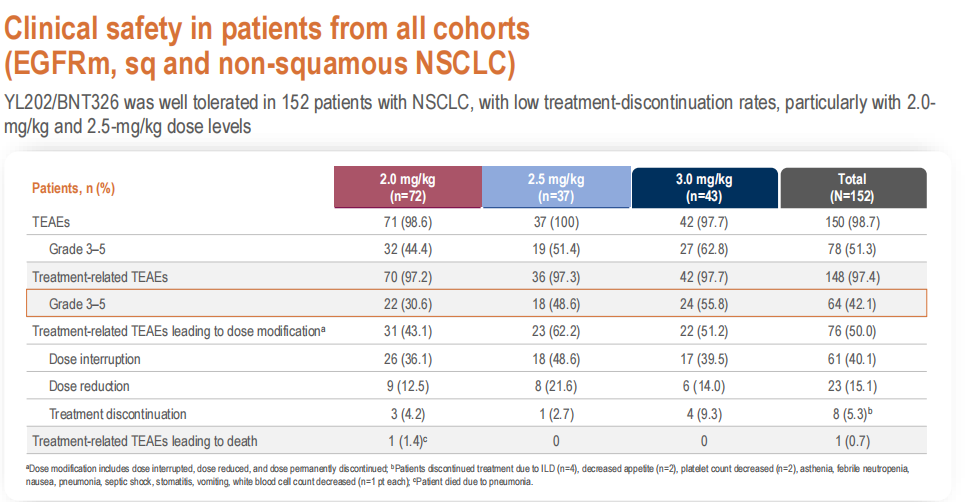
本次 II 期研究结果显示,YL202/BNT326 单药在 NSCLC 亚组中展现出令人鼓舞的抗肿瘤活性,2.0 mg/kg 剂量在经标准治疗后的 EGFR 突变患者中,中位 PFS 达 8.1 个月,在非鳞状 NSCLC 且无 AGA 的患者中,cORR 为 46.7%,中位 PFS 达 5.6 个月,鳞状 NSCLC 中,同样实现了 5.5 个月的中位 PFS。此外,该药物在 2.0 mg/kg 剂量下安全性可控,以上数据支持进一步探索该 HER3 ADC 联合 PD-L1 × VEGF 双特异性抗体治疗 NSCLC。
Q1:从本次披露的 YL202/BNT326(HER3 ADC)数据来看,该药物在疗效和安全性上的核心优势是什么?
刘海峰教授:
YL202/BNT326 是一款靶向 HER3 的 ADC,本次公布的数据显示,YL202/BNT326 在 NSCLC 各亚型中展现出卓越疗效。
具体而言,在经 EGFR-TKI 联合含铂化疗治疗的 EGFR 突变 NSCLC 患者中,2.0 mg/kg 剂量组的中位 PFS 超过 8 个月;在 AGA 阴性的非鳞状 NSCLC 患者中,cORR 达到 46.7%;同时,在鳞状 NSCLC 患者中也观察到了积极的疗效信号。
安全性方面,YL202/BNT326 通过充分的剂量探索,在 2.0 mg/kg 的 III 期推荐剂量下观察到了「低毒高效」的治疗反应:≥3 级贫血、中性粒细胞减少和血小板减少发生率均低于 5%,任意级别黏膜炎发生率仅约 10%,显著优于同类 ADC 药物,为患者提供了耐受性更优的治疗选择。
Q2:当前,全球 ADC 领域的研发呈现出哪些新的突破方向?相较于国际同类研究,YL202/BNT326 的研发设计的中国特色体现在哪里?
刘海峰教授:
从本次 ELCC 大会公布的结果来看,全球 ADC 研发呈现出「后线突破、一线前移」的明确趋势,既有 ADC 单药的后线治疗数据,也有其联合疗法向一线治疗推进的探索。
YL202/BNT326 作为一款中国自主研发的新型 HER3 ADC,其设计及研发过程兼具中国特色与国际视野:相较于国际同类药物,其临床数据主要来源于中国多中心研究,并同时在美国、欧洲、澳洲等全球多地区积累数百例多瘤种、多人群的国际多中心数据。
在研发策略上,YL202/BNT326 早期 I/II 期临床研究实现了充分地剂量优化,国际多中心、多瘤种和多人群中的疗效数据拓展、ADC 单药后线治疗与联合一线治疗方案同步探索。
在国际化布局方面,YL202/BNT326 正在积极推进与 Pumitamig (PDL1/VEGF 双特异性抗体)联合治疗在 NSCLC 一线治疗中的探索,旨在通过差异化联合策略,为晚期 NSCLC 患者提供潜在的一线治疗新选择,并加速该药物在全球范围内的临床转化。
Q2:您认为 YL202/BNT326 未来将如何加速进入国际 NSCLC 临床实践?这对中国乃至全球晚期肺癌患者的治疗格局,会带来怎样的长远影响?
刘海峰教授:
基于本次 ELCC 公布的 II 期临床研究的积极数据,YL202/BNT326 正加速推进其国内外临床研究。
在 EGFR 突变 NSCLC 后线治疗领域,相关 III 期临床试验已启动;在 AGA 阴性非鳞状 NSCLC 一线治疗中,YL202/BNT326 联合 PD-L1/VEGF 双特异性抗体的 II 期研究正在进行,后续将与美国食品药品监督管理局(FDA)和中国国家药品监督管理局药品审评中心(CDE)沟通,推动全球 III 期试验开展;此外,在 EGFR 突变 NSCLC 的一线治疗领域,YL202/BNT326 联合 TKI 方案也已有布局。
随着各项临床试验的顺利推进,YL202/BNT326 有望凭借其在 NSCLC 领域中广谱的疗效、以及低血液学毒性和低黏膜炎发生率的差异化优势,为晚期肺癌患者提供一种更有效且安全性可控的全新治疗选择。这不仅将进一步丰富全球肺癌的治疗格局,也将有力推动中国原研创新药物走向国际舞台。
刘海峰 教授
吉林省肿瘤医院 主任医师、博士生导师
吉林省肿瘤医院党委书记
吉林省抗癌协会理事长
吉林省癌症中心主任
吉林省肿瘤医院药物临床试验机构主任
吉林省肿瘤医院肿瘤转化医学实验室主任
中国医院协会肿瘤医院分会常委
中国抗癌协会整合肿瘤心脏病学分会常委
吉林省抗癌协会整合肿瘤心脏病专业委员会主任委员
吉林省药学会临床试验专业委员会副主任委员
全国先进工作者、全国优秀党务工作者、《中国卫生》「推进医改,服务百姓健康」十大新闻人物

